پیوند هیدروژنی مولکول های آب
چگونه و چرا آب بسیاری از مولکول های قطبی و باردار را حل می کند؟
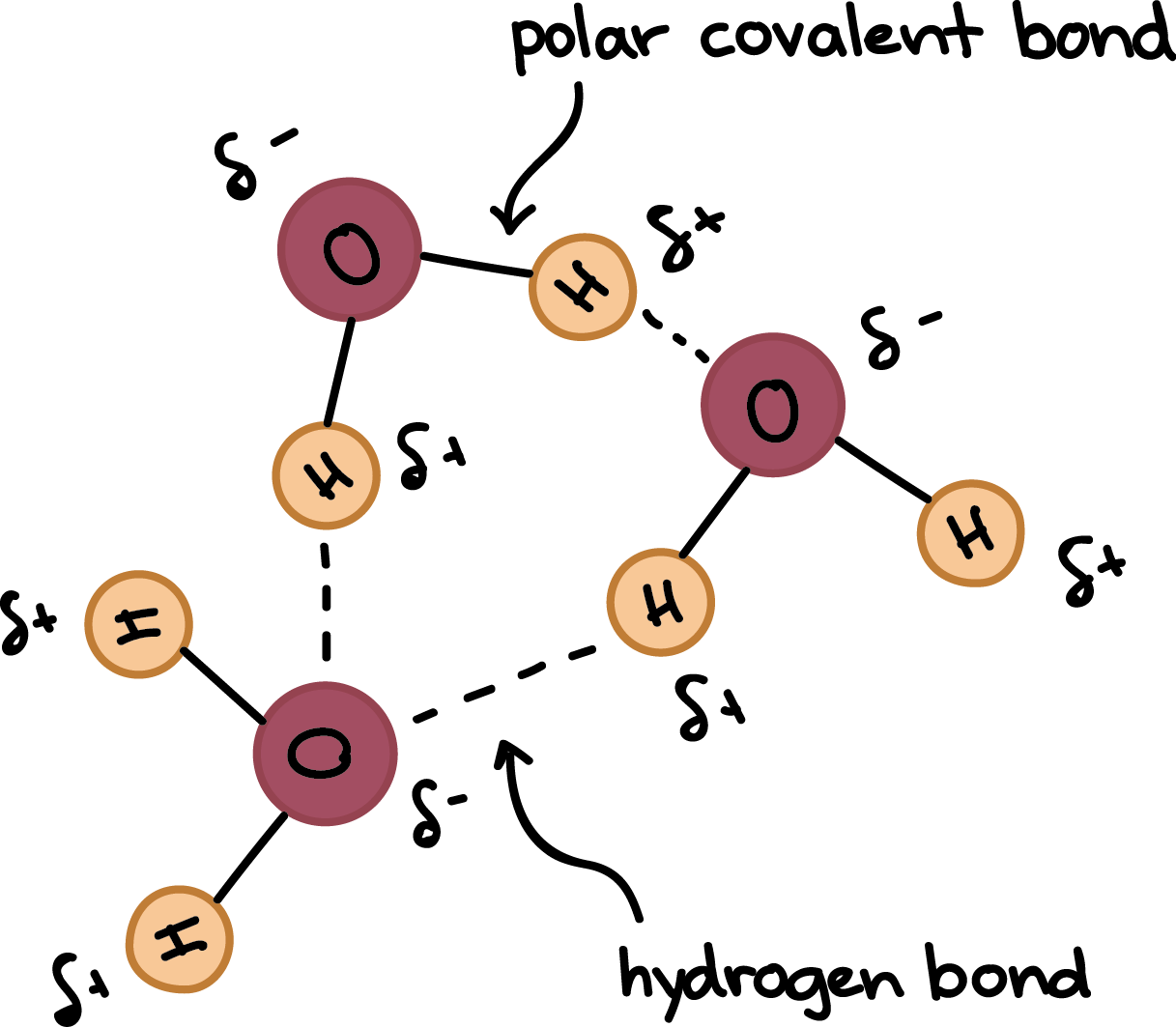 به لطف قطبیت خود، مولکول های آب با خوشحالی یکدیگر را جذب می کنند. انتهای مثبت یک - یک اتم هیدروژن - با انتهای منفی دیگری - یک اتم اکسیژن مرتبط است. این جاذبهها نمونهای از پیوندهای هیدروژنی هستند، برهمکنشهای ضعیفی که بین یک هیدروژن با بار مثبت جزئی و یک اتم الکترونگاتیوتر مانند اکسیژن تشکیل میشوند. اتم های هیدروژن درگیر در پیوند هیدروژنی باید به اتم های الکترونگاتیو مانند O، N یا F متصل شوند.
به لطف قطبیت خود، مولکول های آب با خوشحالی یکدیگر را جذب می کنند. انتهای مثبت یک - یک اتم هیدروژن - با انتهای منفی دیگری - یک اتم اکسیژن مرتبط است. این جاذبهها نمونهای از پیوندهای هیدروژنی هستند، برهمکنشهای ضعیفی که بین یک هیدروژن با بار مثبت جزئی و یک اتم الکترونگاتیوتر مانند اکسیژن تشکیل میشوند. اتم های هیدروژن درگیر در پیوند هیدروژنی باید به اتم های الکترونگاتیو مانند O، N یا F متصل شوند.
مولکول های آب نیز به مولکول های قطبی دیگر و یون ها جذب می شوند. به یک ماده باردار یا قطبی که با آب برهمکنش دارد و در آن حل می شود hydrophilic (آبدوست) گفته می شود: hydro به معنای «آب» و philic به معنای «دوست داشتن» است.
در مقابل، مولکولهای غیرقطبی مانند روغنها و چربیها به خوبی با آب تعامل ندارند. آنها به جای حل شدن در آن از آن جدا می شوند و hydrophobic (آبگریز) نامیده می شوند: phobic به معنای «ترس» است. شاید به این نکته به عنوان یک ویژگی نه چندان مفید سس سالاد با روغن و سرکه توجه کرده باشید. سرکه در اصل فقط آب با کمی اسید است.
- لینک منبع
تاریخ: پنجشنبه , 19 اسفند 1400 (11:47)
- گزارش تخلف مطلب
